发布时间:2023-10-11 | 来源:统计科学研究室
2型糖尿病(T2D)是复杂、慢性、渐进且无法自愈的疾病,它的治疗是一个非常有挑战性的难题。中国现有超过1亿的2型糖尿病患者,还有更多的人处于糖尿病前期的状态。然而,其中相当大一部分的人并不了解自己的风险和健康状况。
除胰岛素抵抗外,胰岛功能衰竭也是2型糖尿病的一个关键特征。为了深入了解2型糖尿病发病过程中胰岛的病理,中国科学院数学与系统科学研究院李雷博士领导的研究团队开发了一种计算方法,对T2D 的动物模型Goto-Kakizaki(GK)和对照模型Wistar(WST)大鼠胰岛的时间序列全基因表达谱以及来自捐献者的人类胰岛的全基因表达谱进行了整合分析。全部数据都来自公共数据库(https://www.ncbi.nlm.nih.gov/geo/),其中大鼠数据来自中国科学院(GSE81811),人的胰岛来自北欧胰岛移植计划(GEO GSE38642)。
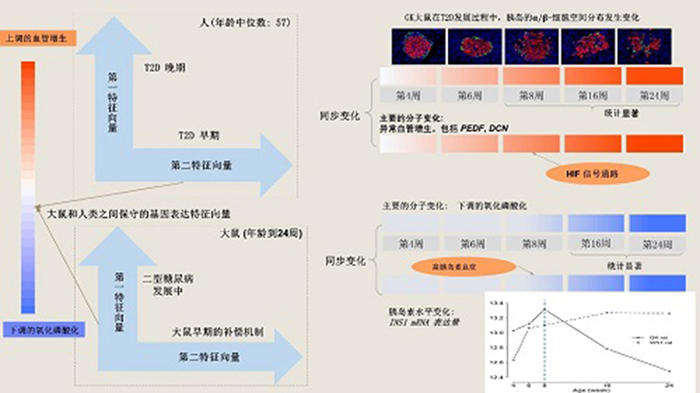
基于表达谱的双重特征结构,整合分析识别出了在两个物种中保守的一个主要基因特征向量,它的特征是上调的血管生成和下调的氧化磷酸化。对于GK和WST大鼠胰岛的表达谱,通过在每一个时间点实施两样本对照统计检验,可以直接验证基因表达的上述改变。在胰岛中,β细胞和α细胞分别分泌降血糖的和升血糖的胰岛素和胰高血糖素。整合分析发现,在转录组层面的血管生成的改变与α/β-细胞分布的改变同步发生,它们早于氧化磷酸化的下调,而后者与胰岛素分泌逐步恶化同步。此外,在GK大鼠中,在胰岛素分泌恶化之前可以观察到显著的高胰岛素血症。
缺氧诱导因子(HIF)信号传导通路是激活血管生成基因转录的上游调控路径。根据整合的表达特征,HIF通路中的大部分基因明显上调。此研究中的多项证据表明,在2型糖尿病发展过程中,HIF信号通路是在缺氧应激下发挥作用。此外,抗血管生成基因THBS1和PEDF在基因特征向量中表达排名靠前,表明存在一种对抗机制。这个转录组层面的对抗机制与在T2D的胰岛中观察到的毛细血管增厚与断裂是一致的。
α/β-细胞分布的改变和高胰岛素血症早于胰岛素分泌恶化的观察结果支持了我们先前的提出的观点:即对糖尿病前期的筛查除了测量血糖水平以外,还应该包括空腹和餐后血胰岛素水平;此外,为了防止胰岛形态的改变进入不可逆的阶段,或者防止2型糖尿病的病理进展变得不可逆,在高胰岛素血症阶段,甚至在血糖水平尚未出现明显异常的情况下,就应该采取积极的干预措施。
该文章已被PLOS ONE 杂志接受发表。
除了公开的原始数据外,计算代码和中间计算数据已存放在开放云平台 https://codeocean.com和 https://zenodo.org,
所有报道的结果都可以复制再现。